COMMENT LA MASSE VOLUMIQUE PEUT VARIER
|
As-tu déjà essyé de verser de la mélasse dehors au mois de Janvier?
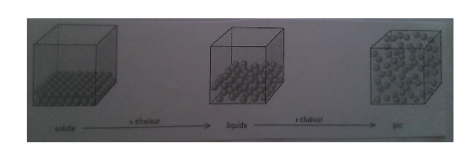
Tu constaterais le ralentissement de l’écoulement lors d’une baisse de température. Si un fluide refroidit, le mouvement de ses particules ralenti et celles-ci se rapprochent les unes de autres. Le fluide se coprime et son volume baisse. Sa masse volumique s’accroit alors. |
Rappelle-toi la formule Mv = M
V M (masse) est invariable et V (volume) diminue, de sorte que M augmente. |
|
En effet, les basses températures accroissent donc la viscosité car le flux des particules devient difficile. Comme tu t’en doutes, une hausse de la température produit l’effet contraire.
Lorsqu’un fluide est chauffée, sa masse volumique décroît et l’écoulement s’accélère. |
La masse volumique restait inchangé pour chacun de ces fluides.
Chaque gaz possède également sa propre masse volumique. L’hélium flotterai au dessus de l’air de la même manière que la pétrole flotte à la surface de l’eau. Sa masse volumique est inférieure à celle de l’air. De même, la masse volumique des solides et propre à chacun d’eau. Ansi, celle des solides qui flottait à la surface de l’eau n’atteint pas 1,00 g/ml. |
EFFET DES VARIATIONS DE TEMPÉRATURE EXPLIQUÉ PAR LA THÉORIE ATOMIQUE:
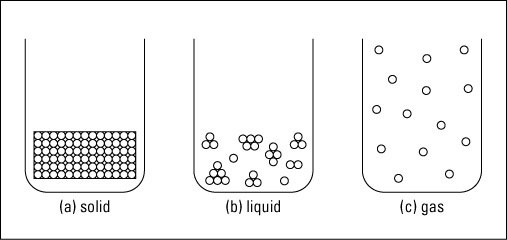
Au niveau macroscopique, (le niveau auquel vous observer directement avec vos yeux), un solide a une forme définie et occupe un volume défini. Pensez à un cube de glace dans un verre - il est un solide. Vous pouvez facilement peser le cube de glace et de mesurer son volume. Au niveau microscopique (où les articles sont si petits que les gens ne peuvent pas observer directement entre eux), les particules qui composent la glace sont très rapprochées et ne déplacent pas beaucoup. Dans un solide, les particules sont compactées et maintenus dans une structure rigide par la force d’attraction. Elles peuvent bouger, mais seulement par vibration sur place. Le réchauffement d’Un solide active les particules qui vibrent plus rapidement. Une augmentation de la chaleur accéère la vibration à un point tel que la force d’attraction ne peut retenir les particules ensemble. La raison pour laquelle les particules qui composent la glace (également connu sous le nom de molécules d'eau) sont rapprochés et ont peu de mouvement est parce que, dans beaucoup de matières solides, les particules sont gardés en un matériau rigide, un réseau cristallin. Les particules qui sont contenus dans le réseau cristallin sont toujours en mouvement, mais à peine - il est plus d'une légère vibration. |
Dans un solide, les particules sont compactées et maintenus dans une structure rigide par la force d’attraction. Elles peuvent bouger, mais seulement par vibration sur place. Le réchauffement d’un solide active les particules qui vibrent plus rapidement. Une augmentation de la chaleur accéère la vibration à un point tel que la force d’attraction ne peut retenir les particules ensemble.
|