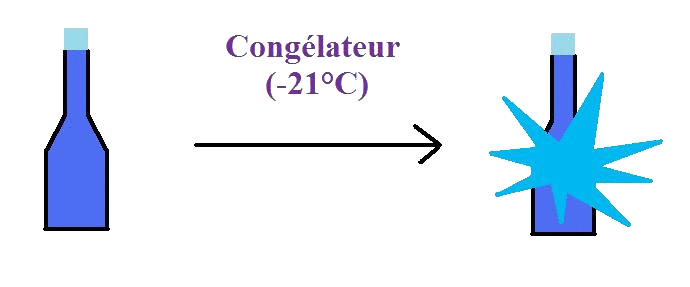L'EAU ET LA MASSE VOLUMIQUE
|
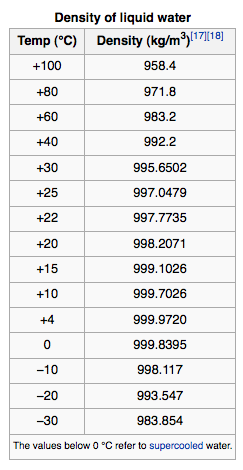
Le suivant c'est un tableau qui démontre la masse volumique de l'eau lors subit à des températures différents.
Notez que lorsque la température augmente, la masse volumique augmente diminue. Cependant, lors que la température descend, sa masse volumique diminue aussi? CE DERNIER NE FAIT PAS DE SENS!! C'est à cause que l'eau, c'est une exception de les lois de la masse volumique et la température. La densité de l'eau liquide est d'environ 1,0 g / mL. Regardons la masse volumique de l'eau à 25 ° C et comparent les à une température plus élevée, 80 ° C. La masse volumique diminue de 0,9970 g / mL à 0,9718 lorsqu'il est chauffé. Cela fait du sens parce que, comme la chaleur est ajoutée à l'eau liquide, il ya une plus grande énergie cinétique des molécules et il ya aussi plus de vibrations des molécules d'eau. Ensemble ceux-ci signifient que chaque unité H2O dans de l'eau liquide prend plus d'espace alors que la température augumente.
|
Nous voyons la même tendance allant de l'eau liquide à 25 ° C (0,9970 g / ml) à de l'eau liquide à 4 ° C (0,99997 g / ml). Avec la diminution de la température, la masse volumique augumente.
En dessous de 4 ° C, cependant, la masse volumique diminue à nouveau. Ce dernier va à l'encontre des lois que nous avons expliqué (et qui s'applique avec tout les autres substances). Comment pouvons-nous expliquer cela? |
|
Cela signifie que la glace flotte sur l'eau. Pour toutes les substances, la masse volumique change avec la température. La masse d'un matériau ne change pas, mais le volume ou espace qu'il occupe, soit augmente ou diminue avec la température. La vibration des molécules augmente à mesure que la température augmente et ils absorbent plus d'énergie.
|
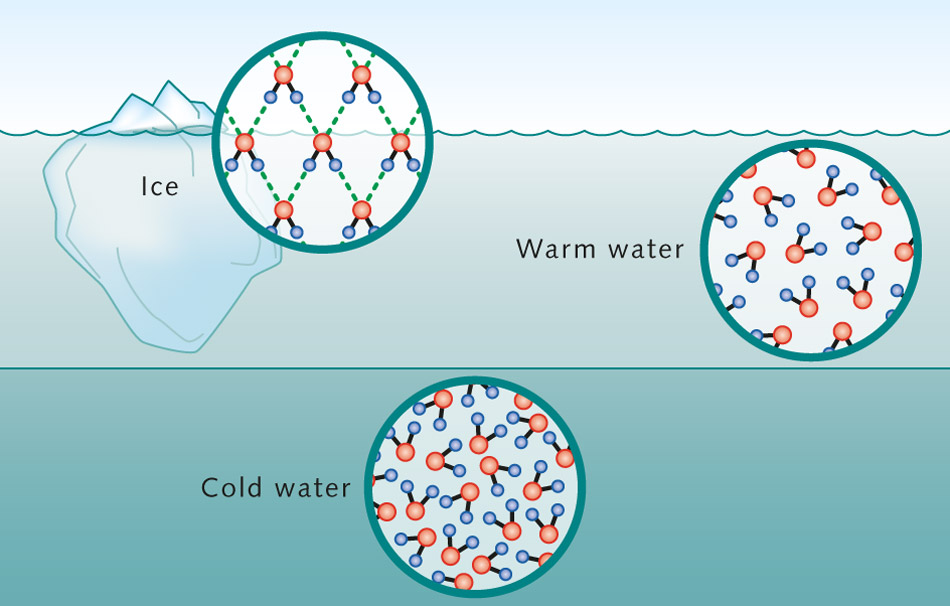
Cependant, cet effet est contradit dans l'eau à cause de la liaison hydrogène. Dans l'eau liquide, des liaisons hydrogène se connectent chaque molécule d'eau à environ 3,4 autres molécules d'eau. Lorsque l'eau gèle en glace, il cristallise en un treillis rigide qui augmente l'espace entre les molécules, chaque molécule d'hydrogène est lié alors à 4 autres molécules.
Ce dernier signifie que le volume s'agrandit et abaisse alors la masse volumique. La faible masse volumique de l'eau sous sa forme solide est due à la façon dont les liaisons hydrogène sont orientés lorsqu'il gèle: les molécules d'eau sont poussés plus loin que celle de l'eau liquide. |
LA GLACE FLOTTE SUR L'EAU
|
Cette propriété unique empêche les lacs de geler totalement en hiver. L’eau qui refroidit descend vers le fond. La température à la partie la plus profonde du lac atteindra 4°C. Elle reste liquide. La vie aquatique peut ainsi survivre. La couche de glace qui recouvre la surface de l’eau joue le rôle d’isolant.
|
Tu sais déjà sans doute que lorsque tu plonges dans un lac, la couche supérieure de l’eau est plus chaude que les couches inférieures. Au cours de l’été, l’eau plus chaude monte à la surface parce qu’elle est moins dense. Toutefois, lorsque la température descend au-dessous de 4°C, la masse volumique de l’eau diminue de nouveau.
La Masse volumique de la glace (0°C) est inférieure à celle de l’eau liquide (4°C). http://bv.alloprof.qc.ca/s1017.aspx |
Si la glace ne flottait pas et coulait cela aurait de grande conséquence pour la vie dans les océans et les lacs.
Cela entraînerait la mort de presque tous les organismes vivants présents dans l’eau car ils ne survivraient pas congelés.
Mais comme la glace flotte, elle protège la vie en isolant la couche d’eau liquide de l’air externe en l’empêchant de geler.
La vie peut y persister et attendre des jours plus cléments, même si la température de l’eau est très basse.
Cela entraînerait la mort de presque tous les organismes vivants présents dans l’eau car ils ne survivraient pas congelés.
Mais comme la glace flotte, elle protège la vie en isolant la couche d’eau liquide de l’air externe en l’empêchant de geler.
La vie peut y persister et attendre des jours plus cléments, même si la température de l’eau est très basse.
QUELLE PORTION D'UN ICEBERG EST IMMERGÉ
|
Environ 90% d’un iceberg se trouve sous la surface de l’eau. La partie visible des icebergs représentent que 10%, ceux-ci constituent un grand danger pour la navigation maritime. Si tu ajoutes un cube de glace dans un verre d’eau, le cube flotte à la surface et une partie est immergée. Tu peux calculer la proportion d’un iceberg qui est imergée en établissant une comparaison entre la masse volumique de la glace et celle de l’eau salée comme suit:
|
Masse volumique de la glace x100
Masse volumique de l’eau salée 0.92 x100 = 89% 1.03 |
La masse volumique explique aussi pourquoi la plupart d'un iceberg se trouve sous la surface de l'océan. Parce que les masses volumiques de glace et de l'eau de mer sont si proches en valeur, la glace flotte "faiblement" dans l'eau. Rappelons que la masse volumique de la glace est de 0,92 g / ml, et la masse volumique de l'eau est de 1,0 g / mL (1,03 pour l'eau salée). Cela signifie que la glace est 90% de la densité de l'eau - et ainsi de 90% de l'iceberg est en dessous de la surface de l'eau.
Bien sûr, il ya quelques petites variations qui affectent le pourcentage exact de l'iceberg sous l'eau. Le icebergs peuvent contenir des sédiments, de la poussière et d'autres particules ramassé par le glacier auparavant. Ils peuvent aussi avoir la croissance des algues sur leur surface immergée. Ces icebergs sont pas une substance pure, et donc leur densité est plus 0,92 g / mL. La température et la salinité de l'eau dans laquelle un iceberg se trouve peut également varier, ce qui signifie que la masse volumique de l'eau de mer ne peut pas être exactement 1,03 g / L. Bien que ces variations sont communs, ils ne changent pas les masses volumiques beaucoup - et ainsi de 90 pour cent est une bonne estimation pour la partie immergée de l'iceberg!
Bien sûr, il ya quelques petites variations qui affectent le pourcentage exact de l'iceberg sous l'eau. Le icebergs peuvent contenir des sédiments, de la poussière et d'autres particules ramassé par le glacier auparavant. Ils peuvent aussi avoir la croissance des algues sur leur surface immergée. Ces icebergs sont pas une substance pure, et donc leur densité est plus 0,92 g / mL. La température et la salinité de l'eau dans laquelle un iceberg se trouve peut également varier, ce qui signifie que la masse volumique de l'eau de mer ne peut pas être exactement 1,03 g / L. Bien que ces variations sont communs, ils ne changent pas les masses volumiques beaucoup - et ainsi de 90 pour cent est une bonne estimation pour la partie immergée de l'iceberg!